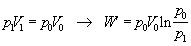Termodynamické procesy
Termodynamické procesy
Na opis rovnovážneho stavu sústavy častíc sa používajú stavové veličiny, ktorých vzájomný súvis vyjadruje stavová rovnica.
V sústave prebiehajúce procesy môžeme rozdeliť z hľadiska ich vratnosti na:
- reverzibilné ( vratné ) procesy - po prebehnutí takéhoto procesu sa sústava môže sama, bez vonkajšieho vplyvu, dostať späť do východiskového stavu. Takým procesom je napríklad veľmi pomalá expanzia plynu uzavretého v nádobe s pohyblivou stenou. A potom opačný proces, veľmi pomalá kompresia tohoto plynu do pôvodného stavu. Proces musí byť tak pomalý, že plyn sa dostáva z počiatočného do konečného stavu a opačne sledom rovnovážnych stavov, ktoré plyn dosahoval po nekonečne malých zmenách týchto rovnovážnych stavov.
- ireverzibilné ( nevratné ) procesy - sústava sa nemôže sama, bez vonkajšieho vplyvu, dostať späť do východzieho stavu. Príkladom takéhoto procesu môže byť prudké stlačenie alebo expanzia plynu v nádobe.
Tieto procesy môžu v prírode prebiehať za rôznych špecifických podmienok.
a) Opíšeme proces prebiehajúci v sústave uzavretej v nádobe s konštantným objemom - izochorický dej. Všeobecne platí, že ak dodáme sústave teplo dQ, toto teplo sa rozdelí na časť dU, ktorá spôsobí zvýšenie vnútornej energie a časť 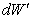 , ktorou vykoná plyn prácu. Teda platí
, ktorou vykoná plyn prácu. Teda platí
Elementárnu zmenu vnútornej energie v tomto vzťahu, množstva n mólov plynu pri zmene teploty o dT, môžeme zapísať 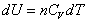 a plynom vykonanú prácu pri zmene objemu o dV vzťahom dW¢ = pdV. Potom prejde vzťah 7.2.3.1 do tvaru
a plynom vykonanú prácu pri zmene objemu o dV vzťahom dW¢ = pdV. Potom prejde vzťah 7.2.3.1 do tvaru
Za danej podmienky, že objem je konštantný (V = konšt.) je zmena objemu nulová (dV = 0 ), teda aj práca vykonaná plynom je nulová (dW¢ = 0 ). Potom sa teplo dodané sústave prejaví len zmenou vnútornej energie. Ak ešte za látkové množstvo dosadíme
vzťah 7.2.3.1 nadobudne tvary
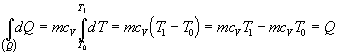 ( 7.2.3.3 )
( 7.2.3.3 )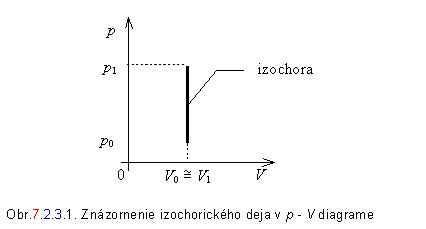
Poslednú rovnicu môžeme slovne vyjadriť takto: Teplo dodané sústave pri izochorickom deji spôsobí len zmenu jej vnútornej energie.
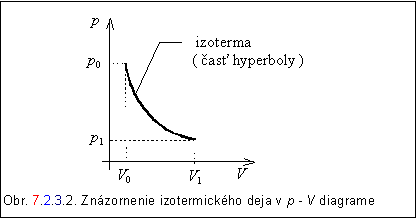
b) Proces prebiehajúci v sústave pri konštantnej teplote - izotermický proces.
Pri sledovaní tohoto procesu budeme vychádzať zo vzťahu 7.2.3.2 .
Za danej podmienky, že teplota je konštantná (T = konšt.) je zmena teploty nulová (dT = 0 ), teda aj zmena vnútornej energie je nulová (dU = 0 ). Potom teplo dodané sústave, sa prejaví ako práca plynu, ktorú vykoná pri svojej expanzii. Rovnica 7.2.3.2 prejde do tvaru
alebo
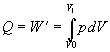
Ak za tlak plynu dosadíme upravenú rovnicu Boylovho - Mariottovho zákona v tvare
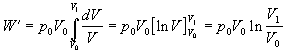
Rovnica opisuje výpočet práce pri známych zmenách hodnôt tlaku a objemu plynu.Túto prácu je možné vypočítať využitím posledného vzťahu aj pri zadaní iných stavových veličín, využitím vhodného tvaru stavovej rovnice. Napríklad
a podobne.
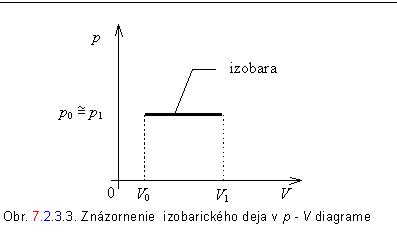
c) Proces pri konštantnom tlaku - izobarický proces.
Za danej podmienky, že tlak je konštantný (p = konšt.) je aj jeho zmena nulová (dp = 0 ). Potom, teplo dodané sústave sa prejaví zvýšením vnútornej energie a prácou, ktorú plyn vykoná pri svojej expanzii. Rovnicu 7.2.3.2 môžeme napísať v tvare
alebo
V poslednom vzťahu sme označili H = U + pV, kde H sme označili novozavedenú fyzikálnu veličinu nazvanú entalpia sústavy. Jeho integráciou dostaneme
Slovne: Teplo prijaté sústavou za konštantného tlaku sa rovná prírastku entalpie sústavy.
|
|
d) Proces prebiehajúci bez výmeny tepla medzi sústavou a okolím - adiabatický proces. V prírode sa vyskytujúce procesy, ktoré prebiehajú dostatočne rýchlo môžeme považovať za adiabatické.
Za danej podmienky, že teplo dodané sústave je nulové (dQ = 0 ), rovnica 7.2.3.1 nadobúda tvar
alebo
Nájdime teraz diferenciály oboch strán stavovej rovnice pV = nRT za podmienky, že n,R sú konštanty a vyjadrime z nej diferenciál teploty
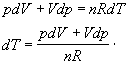
Dosadením do rovnice 7.2.3.4 za dT upravíme vzniknutý vzťah jednoduchými matematickými úpravami
Poslednú úpravu sme vykonali využitím platnosti rovnice
paragraf 7.1.5. Ďalej vykonáme separáciu premenných a rovnicu zintegrujeme ako neurčitý integrál
kde lnC je zvolená integračná konštanta. Využijeme poznaty z matematiky o odlogaritmovaní a dostávame
Vzťah 7.2.3.5 nazývame Poissonova rovnica. Udáva vzájomnú závislosť tlaku a objemu plynu pri adiabatických zmenách. Vzťah môžeme napísať aj v nasledujúcom tvare
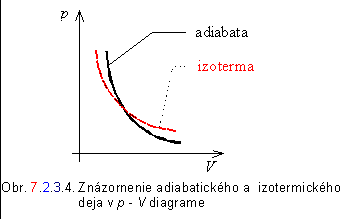
Grafickú závislosť tlaku a objemu pri adiabatickom deji a na porovnanie aj pri izotermickom deji znázorňuje obr. 7.2.3.4.
Príklad 7.2.3.1
Akú hmotnosť má hélium ( molárna hmotnosť M = 4.10-3 kg.mol-1 ), ktoré sme zohriali dodaním tepla 209 J z teploty 60 0C na 80 0C pri konštantnom objeme ?
Riešenie
V súlade so zadaním označíme Q = 209 J, t1 = 60 0C a t2 = 80 0C. Pre výpočet použijeme vzťah 7.2.3.3 v tvare
Úpravou Mayerovho vzťahu 4.2.2.3 získame vzťah pre výpočet cV :
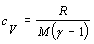
Pri úprave sme využili vzťah pre výpočet Poissonovej konštanty 7.1.14 . Po dosadení do východzieho vzťahu dostávame :
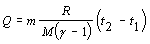
Vzťah matematicky upravíme a dosadíme číselné hodnoty. Hodnotu Poissonovej konštanty vypočítame využitím empirického vzťahu 7.1.14, pričom zo zadania príkladu vieme, že počet stupňov voľnosti i = 3. Prevod teploty z Celziovej na Kelvinovu sme urobili ako v príklade 7.2.1.2 .
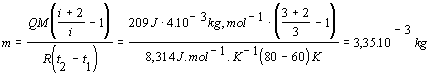
Za daných podmienok sme zohriali 3,35.10-3 kg hélia.
Kontrolné otázky
- Aký je rozdiel medzi reverzibilným a ireverzibilným procesom?
- Prečo pri izochorickom deji plyn prácu nemôže konať?
- Čo nazývame entalpiou sústavy?
- Aká je fyzikálna jednotka entalpie?
- Akú rovnicu by ste považovali pri izotermickom deji za ekvivalent Poissonovej rovnice pri adiabatickom deji?
- Izobaricky zohrejme 5kg oxidu uhličitého z 10°C tak, aby počas rozpínania vykonal prácu 49050J. Na akú výslednú teplotu sa plyn zohreje? Molárna hmotnosť oxidu uhličitého je 44.10 -3 kg.mol -1. (T=334,9K)
- Do nádoby s pevnými stenami umiestnime 20 l vodíka. Koľko tepla mu musíme dodať, aby sa jeho tlak zvýšil z 5066,25kPa na 6079,5kPa? Vodík má molárnu hmotnosť 2.10 -3 kg.mol -1 a hmotnostnú tepelnú kapacitu 10130 J.kg -1.K -1. ( Q=49,383kJ )
- Počas stláčania 5 l vzduchu z počiatočného tlaku 101kPa sa odovzdal okoliu 1kJ tepla. Aký mal tlak a aký objem zaberal vzduch po stlačení, ak dej prebiehal izotermicky? ( p=731,88kPa, V=6,9.10 -4 m3 )
- Akú prácu vykoná 2,5m3 vzduchu s teplotou 32°C a tlakom 455962Pa, keď sa adiabaticky rozopne tak, že jeho teplota klesne na 15°C. Hmotnostná tepelná kapacita vzduchu je 728 J.kg -1.K -1 a molárna hmotnosť je 28,45.10 -3 kg.mol -1. ( W=158,5kJ )