 Entropia, druhá a tretia veta termodynamická
Entropia, druhá a tretia veta termodynamická
Pre účinnosť tepelného stroja, ktorého kruhový dej medzi teplotami T1 a T2 (T2< T1) opisuje reverzibilný Carnotov cyklus, platí
Ak označíme 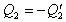 , potom
, potom
alebo po matematickej úprave
Ak podiel Q /T nazveme redukované teplo, vzťah môžeme vyjadriť slovami: Súčet redukovaných tepiel prijatých sústavou počas reverzibilného Carnotovho cyklu sa rovná nule.
Poslednú rovnicu môžeme zovšeobecniť aj na procesy, kedy sústava vratne prijíma teplo viac ako dvakrát
kde N je počet prijatí tepla.
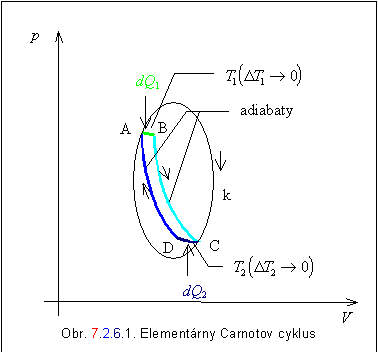
Majme teraz reverzibilný kruhový dej ako na obrázku 7.2.6.1. Plochu ohraničenú do seba uzavretou krivkou k možno vymedziť elementárnymi Carnotovými cyklami, ako napríklad cyklus ABCD. Pri konštantnej teplote T1 sústava prijíma teplo dQ1 a pri konštantnej teplote T2 prijme teplo dQ2 .Aj pre takýto elementárny Carnotov cyklus platí rovnica 7.2.6.1. Rovnicu môžeme zovšeobecniť na všetky elementárne Carnotove cykly vytvorené na ploche ohraničenej krivkou k , teda
V rovnici je dQ teplo vratne prijaté pri teplote T a integrácia sa vzťahuje na celý kruhový dej.
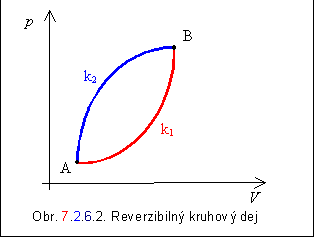
Sledujme kruhový reverzibilný dej, ktorý prebehol medzi bodmi A a B po krivkách k1 a k2, ako na obrázku 7.2.6.2 . Na základe platnosti rovnice 7.2.6.2, môžeme pre tento kruhový dej rozpísať nasledovne
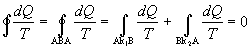
alebo
Na základe posledných vzťahov môžeme usúdiť, že výsledok integrálu nezávisí od spôsobu ako sústava prešla zo základného stavu A do stavu B, ale závisí len od týchto stavov. Ak označíme
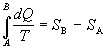
potom veličinu S nazývame entropiou. Jednotkou entropie je joule na kelvin [J.K-1]. Jej diferenciál je
Ak prebehne v sústave kruhový dej reverzibilne a sústava sa dostane do východzieho bodu, rovnicu (7.2.6.3 ) môžeme prepísať do tvaru
ktorý je považovaný za matematickú formuláciu druhej vety termodynamickej.
Druhá veta termodynamická umožnila entropiu S definovať len ako funkciu stavu sústavy.
Pri sledovaní entropie adiabatických (dQ=0) reverzibilných dejov zapíšeme zmenu entropie nasledovne
Pre entropiu pri zmene stavu sústavy z A do B potom platí
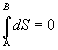
Po integrácii a matematickej úprave
SB - SA = 0
SA = SB
Posledý vzťah môžeme slovami vyjadriť: Počas adiabatických reverzibilných dejov sa entropia sústavy nemení.
Gibbs tieto vratné adiabatické deje nazval izentropické deje.
Vo viacerých učebniciach fyziky by sme našli matematické postupy ktoré dokazujú, že účinnosť tepelných strojov založených na reverzibilnom Carnotovom cykle je najvyššia. Teda účinnosť tepelných strojov založených na ireverzibilnom deji je vždy menšia. Preto platí
Ak označíme 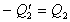 a rovnicu upravíme, dostávame tvar
a rovnicu upravíme, dostávame tvar
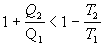
a po úprave
Poslednú rovnicu môžeme zovšeobecniť aj na proces, kedy sústava prijíma teplo viackrát
kde N je počet prijatí tepla. A pre ireverzibilný kruhový dej prebiehajúci spojite platí
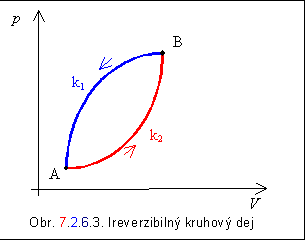
Majme teraz ireverzibilný kruhový dej prebiehajúci medzi bodmi A a B ako na obrázku 7.2.6.3. Dej prebieha z bodu B do bodu A po krivke k1 reverzibilne a z bodu A do B po krivke k2 ireverzibilne. Pre tento dej platí
Po úprave integračných hraníc môžeme napísať
Z predchádzajúcich poznatkov o narastaní entropie pre reverzibilné deje platí
a s použitím vzťahu 7.2.6.4 prechádza posledná rovnica do tvaru
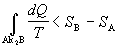
Pri sledovaní entropie adiabatických (dQ = 0) ireverzibilných dejov potom môžeme písať
alebo
Posledný vzťah môžeme slovami vyjadriť nasledovne: Pri všetkých ireverzibilných dejoch prebiehajúcich v sústavách od okolia tepelne izolovaných sa entropia sústavy zväčšuje.
Sústavou pokusov pri teplotách T® 0 sa zistilo, že niektoré vlastnosti látok ( elektrický odpor vodičov, teplotná rozťažnosť, molárna tepelná kapacita) nie sú závislé od teploty. Alebo opačne - zmenou žiadnych vonkajších parametrov látky pri teplote T® 0 nemožno dosiahnuť zníženie teploty na T = 0 . Túto skutočnosť
Planck vyjadril vetou:
Čistú tuhú látku nie je možné konečným procesom ochladiť na nulovú Kelvinovu teplotu.
Je pravdepodobné, že v blízkosti teploty T = 0 prestáva tepelný pohyb častíc, čiže aj už existujúce nerovnovážne stavy v sústave môžu existovať ľubovolne dlho. Tieto poznatky zovšeobecnil Nernst v tretej vete termodynamickej. Jej znenie je:
Pre ľubovoľný izotermický dej prebiehajúci pri teplote T® 0 je zmena entropie nulová. Vetu doplnil Planck tým, že položil entropiu pri teplote T® 0 rovnú nule S(T=0) = 0. Tým odstránil neurčitosť v určení absolútnej hodnoty entropie každého stavu látky.
Príklad 7.2.6.1
Aká je zmena entropie 1 kg vodnej pary zohriatej na 100 0C vzhľadom na stav v kvapalnom skupenstve pri teplote 20 0C ? Hmotnostná tepelná kapacita vody je cV = 4186 J. kg-1.K-1 a skupenské teplo vyparovania vody lV = 2,256.106 J. kg-1.
Riešenie
Sledovanú zmenu entropie môžeme rozdeliť na dve časti. Zmena entropie m = 1kg vody pri jej zohriatí z teploty tA = 20 0C Þ TA = 293,15 K na bod varu tB = 100 0C Þ TB = 373,15 K a zmenu entropie vody počas jej premeny na paru pri konštantnej teplote tB . Celkovú zmenu entropie zapíšeme
Pre výpočet jednotlivých zmien entropie použijeme vzťah 7.2.6.3 a dosadíme
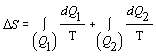
Proces zohrievania vody z teploty TA na TB opíšeme rovnicou dQ1 = mcV dT a vyparenie vody rovnicou dQ2 = lV dm. Pritom nesmieme zabudnúť, že vyparovanie sa deje pri konštantnej teplote TB. Za týchto podmienok zmenu entropie vypočítame
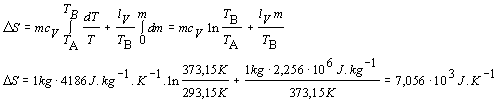
Zmena entropie vodnej pary je 7,056.103 J.K -1 .
Kontrolné otázky
-
Čo hovorí kruhový integrál vo vzťahu 7.2.6.2?
-
Aký je význam druhej vety termodynamickej vo vzťahu k entropii?
-
Aké sú to izentropické deje?
-
Aký je vzťah medzi účinnosťou reverzibilných a ireverzibilných kruhových dejov?
-
Aký bol Planckov príspevok k formulácii tretieho termodynamického zákona?
-
Ako sa zmení entropia liatinového odliatku s hmotnosťou 2t, ak ho ochladíme z 10000C na 500C. Hmotnostná tepelná kapacita liatiny je 544J.kg -1.K -1. ( Ds= -1492kJ.K -1 )
-
O koľko sa zmení entropia 0,1kg ľadu teploty -50C, ak sa zmení na vodu 0 0C teplú.Hmotnostná tepelná kapacita ľadu je 2090J.kg -1.K -1, hmotnostné skupenské teplo topenia ľadu je 333,6.103 J.kg-1. ( Ds=126J.K -1)
